

TECHNICAL SUPPORT
HPLC분석관련
역상크로마토그래피에서 분리를 결정하는 요인(이동상)
역상크로마토그래피에서 분리를 결정하는 요인(2)
고정상 이외의 요인
■ 이동상
유기 용매의 종류·조성 완충 용액의 종류·농도·pH
■ 용질의 성질
화학적 성질(이온성, pka, 용해도)·구조
■ 컬럼온도
역상크로마토그래피에서 분리를 결정하는 주요한 요인이 고정상입니다. 하지만 고정상 외에도 분리를 결정하는 데 주요한 요인이 있습니다. 본 포스트에서는 이런 고정상 이외의 요인에 대해 설명드리고 실례를 들어 개선하는 포인트도 말씀드리겠습니다.
■ 이동상
먼저 이동상 부분입니다. 고정상과 함께 액체크로마토그래피를 이루는 데 중요한 역할을 하는 부분입니다. 역상에서는 다음과 같은 용매들을 사용합니다. 역상크로마토그래피의 대부분은 물, 메탄올, 아세토나이트릴에서 이루어집니다만 용출력이 부족할 경우에는 더 용출력이 높은 용매들을 사용하기도 합니다.
-
역상 모드에서 사용되는 용매의 용출력

* 상용성이 없어"아세트산 에틸/물" 계열은 불가
역상에서 주로 사용하는 용매들의 상대적 강도를 비교해보면 아래 표와 같습니다.
-
유기 용매/물 혼합계의 상대적 용매 강도 1
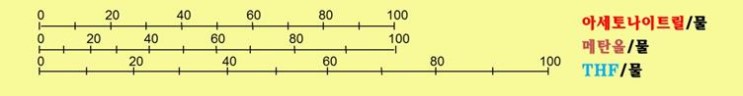
물론 위의 표는 참고가 될 뿐 정확하게 일치한다고 말할 수는 없습니다. 유기 용매/수용액의 혼합, 대상 화합물의 가용성에 따라 달라질 수 있기 때문입니다.
그럼 유기용매 종류의 변경을 통한 최적화 실례를 보여드리겠습니다.
플라보노이드를 분석하는 데 다음과 같은 조건으로 분석을 실시했습니다.

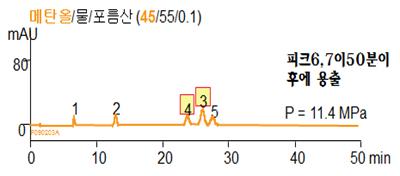
아세토나이트릴을 사용하는 조건입니다. 이를 메탄올을 사용하는 조건으로 변경해 보겠습니다. 조금전에 설명드린 용출력 비교한 것을 바탕으로 함량을 변경시켰습니다. 용출력은 비슷하지만 유기용매 종류에 따른 선택성이 바뀌어서 피크 6, 7이 나오지 않고, 3번과 4번의 용출 순서가 바뀌었습니다.
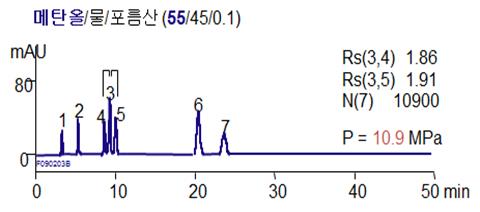
이를 다시 메탄올의 비율을 변경하여 용출시간을 당기고 분리, 분석시간을 최적화 해보았습니다. 3, 4번의 용출순서는 바뀌었지만 전체적인 분석시간은 빨라졌습니다. 물론 압력이 증가하고 3,4 번과 3,5번의 분리능은 떨어졌지만 분석하기에 무리가 없는 조건으로 변경되었습니다.
메탄올, 물 등의 조건만으로 모든 조건을 최적화 시키기에는 무리가 있습니다. 제 2의 유기용매 첨가에 의한 최적화를 진행해보도록 하겠습니다.
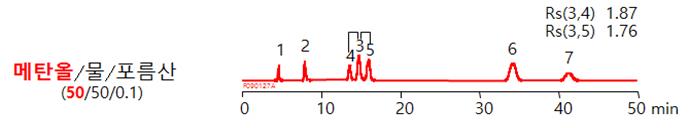
위와 같은 조건에서 유기용매의 총량은 그대로 두고 제 2의 유기용매를 첨가해 보도록 하겠습니다. 첨가할 때는 기존 유기용매양의 10% 정도를 기준으로 시작해보는 것이 좋습니다.
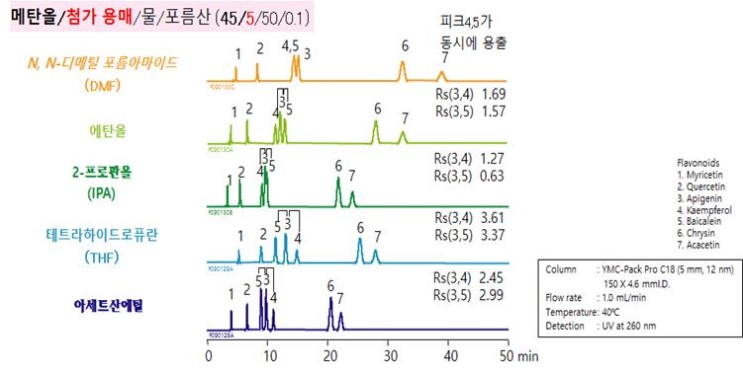
THF를 첨가했을 때 3,4,5번의 분리능이 가장 좋게 나오는 것을 확인할 수 있었습니다.
이외에도 상기 실험에서의 포름산처럼 여러 첨가제가 분리에 도움을 주는 경우가 있습니다.
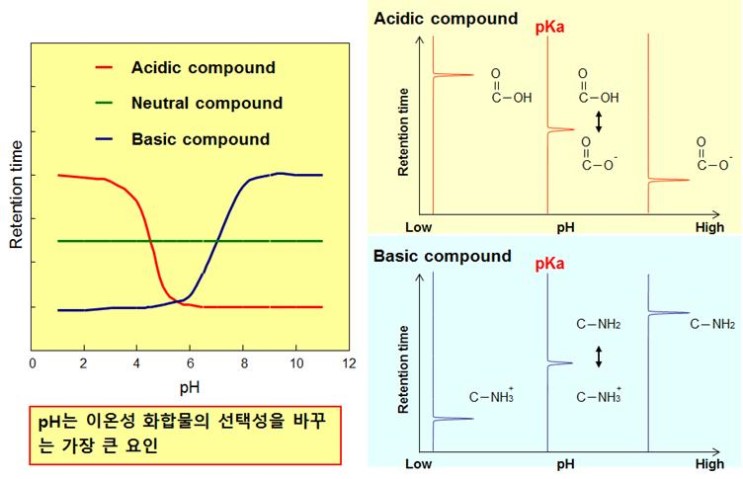
포름산과 같은 첨가제는 이동상에 pH를 조절합니다. 아래의 그림에서와 같이 물질의 용출력은 pH에 따라 많은 차이를 보이는 것을 알 수 있습니다. 특히 분석 물질이 이온성을 가질 경우 그 영향은 매우 큽니다.
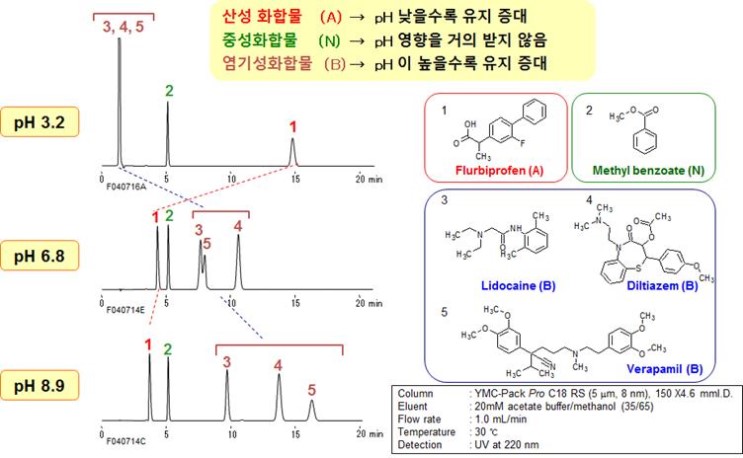
실례를 살펴보겠습니다. 아래는 산성, 염기성 의약품을 분석한 내용입니다. 산성화합물은 pH가 낮을 경우 유지시간이 길어지고, 염기성 화합물은 pH가 높을수록 유지시간이 길어지는 것을 확인할 수 있습니다. 중성화합물은 pH에 영향을 거의 받지 않습니다.
이런 첨가제들을 통해 물질의 선택성을 바꾸고 좋은 데이터를 얻기 위해서는 첨가제의 특징을 잘 알고 사용하여야 합니다. 일반적으로 역상에서 많이 사용하는 완충용액이나 첨가제는 아래의 표와 같습니다. 실험하실 때 참조하셔서 좋은 데이터를 얻으시길 바랍니다.
|
종류 |
pKa |
Buffer range |
일반적인 사용 농도 |
휘발성 (LC/MS이나 분취에 적용) |
|
TFA |
< 1.0 |
0.01~ 0.1% |
○ |
|
|
H3PO4 |
2.1 |
0.01~ 0.1% |
× |
|
|
NH4H2PO4-H3PO4 [NaH2PO4 -H3PO4 , KH2PO4 -H3PO4] |
2.1 |
1.1~3.1 |
5~50 mM (<20 mM권장) |
× |
|
HCOOH |
3.7 |
0.1~1.0% |
○ |
|
|
HCOONH4-HCOOH [HCOONa-HCOOH, HCOOK-HCOOH] |
3.7 |
2.7~4.7 |
5~50 mM |
NH4 salt:○ [Na, K salt:×] |
|
CH3COOH |
4.8 |
0.5~5.0% |
○ |
|
|
CH3COONH4-CH3COOH [CH3COONa-CH3COOH, CH3COOK-CH3COOH] |
4.8 |
3.8~5.8 |
5~50 mM |
NH4 salt:○ [Na, K salt:×] |
|
(NH4)2HPO4 -NaH2PO4 [Na2HPO4 -NaH2PO4, K2HPO4 -KH2PO4] |
7.2 |
6.2~8.2 |
5~50 mM (<20mM권장) |
× |
|
Triethylamine-CH3COOH (TEAA) |
4-6, 10-11 |
○ |
||
|
HCOONH4-NH3, CH3COONH4-NH3 |
9.2 |
8.2~10.2 |
○ |
|
|
Na3PO4 -Na2HPO4, K3HPO4 -K2HPO4 |
12.3 |
11.3~13.3 |
× |
|
|
NH4HCO3-NH3, |
8.5~10.5 |
○ |
컬럼온도는 어떨까요. 근래 시스템들에 컬럼 오븐이 거의 필수인 것처럼 여겨지는 것은 샘플의 분리가 온도에 따라 달라지기 때문입니다. 컬럼 온도에 따른 영향을 확인하기 위해 End capping이 고도화되어 있지 않은 종전 C18컬럼(실리카계열)을 사용해서 물질을 분석해 보았습니다.
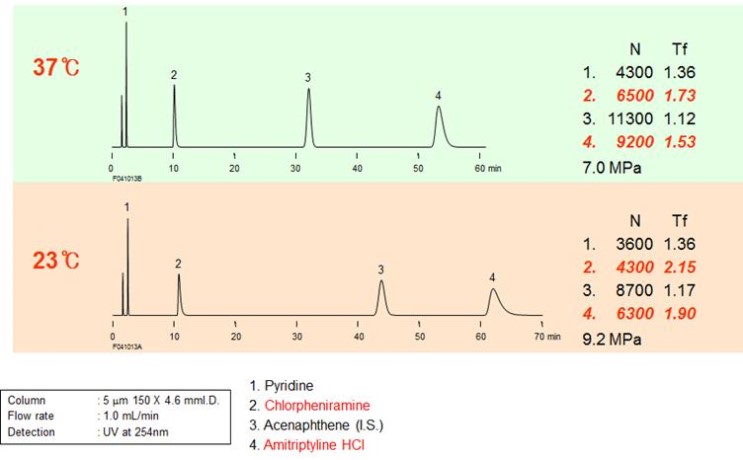
위와 같이 몇몇 화합물들은 온도에 따라 분리에 크게 영향을 미치는 것을 확인할 수 있습니다. 저온에서 특히 염기성 화합물들은 Tailing이 생기기 쉽습니다. 물론 온도는 공기 탈착속도나 이동상의 점도에도 영향을 미치기 때문에 낮은 온도보다는 약간 높은 온도가 분리가 잘 될 가능성이 높습니다. 하지만 모든 샘플에서 동일한 기준을 적용시키기는 어렵기 때문에 샘플에 따라 온도의 영향도 확인해보는 것이 좋습니다.
이상으로 고정상 외의 분리에 미치는 요인을 살펴보았습니다. 분리가 가장 큰 영향을 미치는 것은 고정상이지만 분리의 개선을 위해서는 고정상 외의 조건에 주목할 필요가 있습니다. 이동상의 용출력, pH, 온도 등을 감안해서 최적의 조건을 만들기 위한 수고를 감내해야 합니다.
만점짜리 컬럼은 지구상에 존재하지 않습니다.
컬럼으로 90%정도를 채우고 나머지 10%는 이동상이나 pH, 온도 등을 조절하여 채워간다고 생각하시면 HPLC 분석에 큰 도움이 되리라 생각합니다.
- P.J.Schoenmakers, J. Chromatogr., 185, 179 (1979), P.J.Schoenmakers, J. Chromatogr., 218, 259 (1981)



